Hydrogen sulfide (H2S) và phosphine (PH3) là những chất có mùi khó chịu và rất độc. Trong bài viết này, chúng ta sẽ tìm hiểu về quá trình tạo thành liên kết cộng hóa trị trong hai chất này.
Tạo thành liên kết cộng hóa trị
-
Xét phân tử H2S được tạo từ 2 phi kim:
- Lõi nguyên tử của lưu huỳnh (S) có 6 electron ở lớp vỏ ngoài cùng, do đó nó có xu hướng nhận thêm 2 electron để đạt được cấu hình electron bền vững.
- Tương tự, lõi nguyên tử của hydro (H) có 1 electron ở lớp vỏ ngoài cùng, và nó cũng có xu hướng nhận thêm 1 electron.
-
Xét phân tử PH3 được tạo từ 2 phi kim:
- Lõi nguyên tử của photpho (P) có 5 electron ở lớp vỏ ngoài cùng, và nó cần thêm 3 electron để đạt được cấu hình electron bền vững.
- Hydro (H) cũng có xu hướng nhận thêm 1 electron để đạt cấu hình electron bền vững.
Quá trình tạo thành liên kết cộng hóa trị
-
Trong phân tử H2S, khi 2 nguyên tử hydrogen và 1 nguyên tử lưu huỳnh liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử S góp 2 electron để tạo thành 2 cặp electron dùng chung. Quá trình này được minh họa như hình dưới đây:
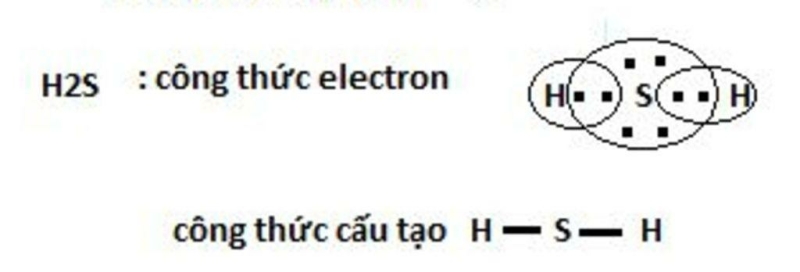
-
Trong phân tử PH3, khi 3 nguyên tử hydrogen và 1 nguyên tử photpho liên kết với nhau, mỗi nguyên tử H góp 1 electron và nguyên tử P góp 3 electron để tạo thành 3 cặp electron dùng chung.
Đây là quá trình tạo thành liên kết cộng hóa trị trong hai chất Hydrogen sulfide (H2S) và phosphine (PH3). Sự tương tác giữa các electron này giúp duy trì cấu trúc phân tử và tính chất của các chất này. Tuy nhiên, cần lưu ý rằng cả H2S và PH3 đều là những chất độc và có mùi khó ngửi, do đó cần hạn chế tiếp xúc với chúng.
Nếu bạn muốn biết thêm về các bài giải khác trong môn Hóa học lớp 10, hãy truy cập Chân trời sáng tạo.
